最近はADC(抗体薬物複合体)の
目覚ましい効果が次々に発表されています。
その中で、注目されている分子に
TROP2があります。
2020年に第一三共がプレスリリースにて
DS-1062の第1相臨床試験における
トリプルネガティブ乳がん患者への
投与開始 について
という発表を行いました。
このDS-1062が
TROP2をターゲットとするADCです。
また アメリカでは2020年4月
FDAに迅速承認を受けている薬が既に存在します。
なんだかスゴそうではありませんか?
 チク子
チク子今回はTROP2について、
くわしく概要を
まとめてみました。
気になる方は
是非およみください!



ちなみに2024年
現在の開発状況は
以下のとおりです。
| 薬剤名 | 販売会社 | 国 | 特徴 |
|---|---|---|---|
| サシツズマブ ゴビテカン) | Gilead Sciences | 米国 | トリプルネガティブ乳がん、進行性尿路上皮がん、 HR+/HER2-乳がんに対して使用。FDATRODELVYの名前で承認済み。 |
| ダトポタマブ デルクステカン | Daiichi Sankyo, AstraZeneca | 日本 英国 | 局所進行または転移性非小細胞肺がん(NSCLC)や 他のがん種に対する臨床試験が進行中。 |
| SKB-264 | Merck, Sichuan Kelun Biotech | 米国 中国 | NSCLCや子宮内膜がんの治療に向けた 臨床試験が進行中。 |
| DB-1305 | DualityBio, BioNTech | 米国 独国 | 進行性固形腫瘍を対象にした臨床試験が進行中。 プラチナ耐性卵巣上皮がんに対するファストトラック指定を受けている。 |
| HMBD-501 | Hanmi Pharmaceutical | 韓国 | 固形腫瘍に対する治療が期待されている。 |
| BAT8003 | Bio-Thera Solutions | 中国 | 様々ながん種に対する臨床試験が進行中。 |
| RC48 | RemeGen | 中国 | 胃がんや尿路上皮がんを含む複数のがん種に対して試験が行われている。 |
TROP2ってなに?
まずは名前の確認です。
名前って大事ですからね。
TROP-2はtrophoblast-surface antigen 2
トロホブラストの最初のTROPをとっています。
最初の単語からしか頭文字取らないやつですね。
和訳すると
栄養芽細胞表面抗原2という感じでしょうか。
個人的にはトロホブラスト細胞の方が
馴染みがあります。



発見自体は1990年ごろで、
かなり歴史自体は
古いタンパクですね。
役割
TROPのメインの役割は
- 細胞間接着
- 小胞体からのカルシウム流出を
促進することで細胞増殖経路をリン酸化
細胞が
くっつく力と増える力を司る
タンパク質です。
この他にも
中間リン酸化経路としての側面もありますが、
直接的に作用するのはこの二つ。
特にがんにおいては、この特性が暴走し、
増殖、遊走、転移、アノイキス耐性に寄与します。



アノイキス?



細胞は決まった場所にくっ付けず、
根無し草になるとアポトーシスして
自死するんです!
それをアノイキスと言うよ。



寂しすぎると
死んじゃうんだね。
アノイキス耐性なので
孤独でも死ななくなる
と言うことね。



孤独でも死滅せず、
結果増えやすくなるため
転移増殖しやすくなる因子
と考えられています。
分布と発現量
TROP-2がいつどこに多くあるかというと、
胚や胎児期に広く分布しています。
特に胚トロポブラスト細胞や胎盤に
多いとされています。
発生初期や胎児期には増殖が必要なので
広範囲にわたって発現していると考えると
しっくり来ますね。
成人になっても
上皮細胞に発現することがわかっていまして、
こっちも日々のダメージから
分裂・増殖を必要とする部分に発現しています。
具体的には皮膚、食道、肺等に
多く発現しています。
なお血球細胞には見つかっておりません。
がん細胞においても
- 肺がん乳がん
- 膵臓がん
- 子宮頸がん
- 卵巣がん
- 大腸がん
- 胃がん
- 前立腺がん
- 食道がん等
等にて高発現しており
発現量が多いと予後不良と
わかっています。



TROP-2が多いと増え易くて、
転移しやすい特徴を持つワケ
だから予後不良には
確かになりやすそう。
小活
- TROP-2は増殖と細胞接着に関与
- 多くのがんで高発現
- 発現量が予後不良因子
- 正常細胞にも存在する
抗TROP-2のADCについて
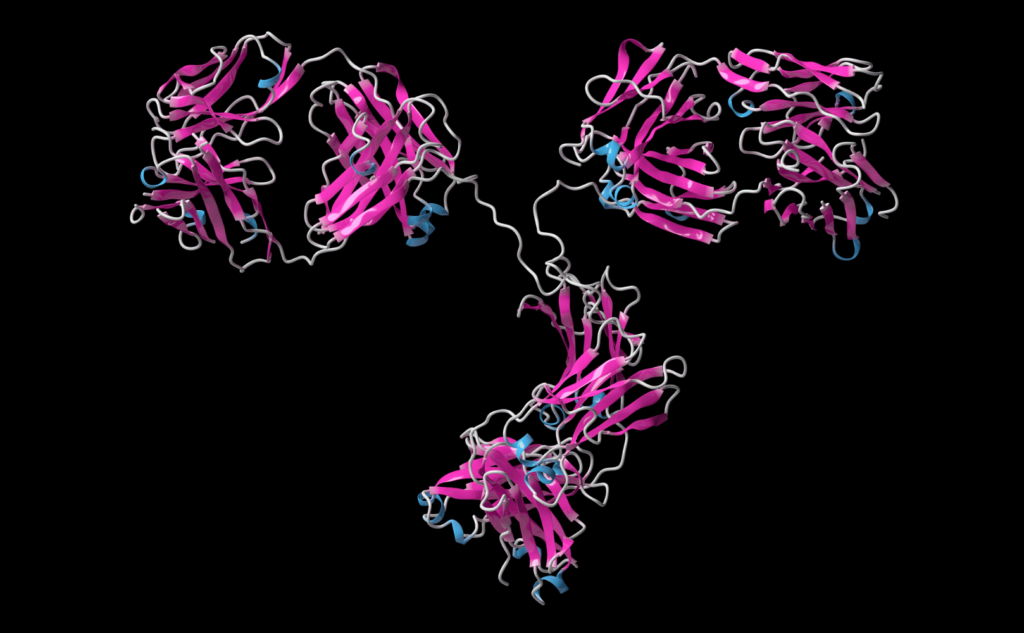

ここからは実際の薬を見ていきます。
TROP-2をターゲットにした薬剤で
開発が進んでいる薬剤が2つあります。
両剤とも日本未承認の抗体薬物複合体です。
1剤は既にアメリカにて承認されています。
一つ目がImmunomedics社にて創薬された
sacituzumab govitecan
(サシツズマブゴビテカン)。
もう一つが第一三共にて開発されている
DS-1062 ダトポタマブ デルクステカンです。
余談ですが1062は
TROP2をもじっています10(T)6(ROP)2



なおADC?
抗体薬物複合体?
DAR?という方は、
先に過去記事をご確認ください


| 薬剤名 | 販売会社 | 国 | 特徴 |
|---|---|---|---|
| サシツズマブ ゴビテカン) | Gilead Sciences | 米国 | トリプルネガティブ乳がん、進行性尿路上皮がん、 HR+/HER2-乳がんに対して使用。FDATRODELVYの名前で承認済み。 |
| ダトポタマブ デルクステカン | Daiichi Sankyo, AstraZeneca | 日本 英国 | 局所進行または転移性非小細胞肺がん(NSCLC)や 他のがん種に対する臨床試験が進行中。 |
| SKB-264 | Merck, Sichuan Kelun Biotech | 米国 中国 | NSCLCや子宮内膜がんの治療に向けた臨床試験が進行中。 |
| DB-1305 | DualityBio, BioNTech | 米国 独国 | 進行性固形腫瘍を対象にした臨床試験が進行中。 プラチナ耐性卵巣上皮がんに対するファストトラック指定を受けている。 |
| HMBD-501 | Hanmi Pharmaceutical | 韓国 | 固形腫瘍に対する治療が期待されている。 |
| BAT8003 | Bio-Thera Solutions | 中国 | 様々ながん種に対する臨床試験が進行中。 |
| RC48 | RemeGen | 中国 | 胃がんや尿路上皮がんを含む複数のがん種に対して試験が行われている。 |
sacituzumab govitecan
(サシツズマブゴヒテカン)
sacituzumab govitecanは
RS7と呼ばれるTROP-2抗体と
SN-38を結合させた抗体薬物複合体です。
イリノテカンは第一三共から
トポテシンという名前で発売されている
抗悪性腫瘍剤でして
2009年より本邦でも発売されている
歴史ある抗悪性腫瘍剤です。
そしてこれは大きな特徴ですが、
薬物抗体比(DAR)はなんと7.6です。
エンハーツに続いて2つ目のDAR約8製品です。
リンカーは細胞内酵素とpH依存で切断されます。
薬物放出力を上げるためかpH依存で
分解されるため血液中での
安定性が少々悪いようです。
そのため血中内でリンカーが外れてしまい、
トポテシンに多く発現する
消化管での副作用が認められています。
抗体薬物複合体の特徴の副作用を抑えるという
特徴を完全には発揮できていない様に感じます。
もともとトポテシンは
血中に注射されている薬なので、
開発会社はリンカー分解され
少々血中で薬物が放出されても
大きな副作用に発展しないと
踏んだのかもしれません。
アメリカではP3試験が進行中でしたが、
P2試験の結果があまりによかったため
有効中止という形が取られ、
少なくとも2レジメンの治療歴を有する
トリプルネガティブ進行乳癌を対象に
迅速承認されています。



販売名はTRODELVYです!
論文紹介:転移性トリプルネガティブ乳がんにおけるサシツズマブゴビテカン
NEJMに2021/4/22に掲載された
無作為化第3相試験の結果を簡単に解説します。
紹介論文:Sacituzumab Govitecan in Metastatic Triple-Negative Breast Cancer
無作為化第3相試験:背景
対象:再発または難治性の転移性トリプルネガティブ乳がん患者(脳転移のない合計468人)
単剤化学療法(エリブリン、ビノレルビン、カペシタビン、またはゲムシタビン)と比較
主要エンドポイント:脳転移のない患者の無増悪生存期間
すべての患者は以前にタキサンを使用
サシツズマブゴビテカン235人に割り当て
化学療法233人に割り当て
結果:有効性
| 項目 | サシツズマブゴビテカン | 化学療法 | ハザード比 |
|---|---|---|---|
| 無増悪生存期間中央値 | 5.6か月 (95%CI 4.3〜6.3; 166イベント) | 1.7か月 (95%CI 1.5〜2.6; 150イベント) | 0.41 (95%CI:0.32〜0.52; P <0.001) |
| 全生存期間中央値 | 12.1か月 (95%CI、10.7〜14.0) | 6.7か月 (95%CI、5.8〜7.7) | 0.48 (95%CI、0.38〜0.59; P <0.001) |
| 客観的反応を示した患者割合 | 35% | 5% | / |
結果:安全性:グレード3以上の主要な治療関連有害事象の発生率
| 項目 | サシツズマブゴビテカン | 化学療法 |
|---|---|---|
| 好中球減少症 | 51% | 33% |
| 白血球減少症 | 10% | 5% |
| 下痢 | 10% | 1%未満 |
| 貧血 | 8% | 5% |
| 発熱性好中球減少症 | 6% | 2% |
| 有害事象による死亡 | 0人 | 3人 |



全生存期間中央値で
圧倒的有効性と
前述のトポテシンの副作用の
下痢が10倍以上
増えていることがわかりますね!
効果は折り紙付きです!
ADCすごい!
ダトポタマブ デルクステカン(DS-1062)
DS-1062は第一三共が開発中のADCです。
sacituzumab govitecanと異なり、
開発はP1の結果が
米国臨床腫瘍学会2020で発表されました。(結果はこちら)登場はまだまだ先になるでしょうし、予期せぬ副作用で中止になるかもしれません。
2024年追記:ガンガンに試験進めまして、
日本でも承認申請がなされました!
この薬はTROP-2版エンハーツとも言える薬です。
抗体はTROP-2抗体、
DARは4と1抗体に4つしか薬物を搭載していない
という違いはあるものの(エンハーツは約8)
エンハーツとリンカーと抗腫瘍薬は全く同じです。
このリンカーは血中で安定し
簡単には薬物を放出しません。
さらにがん細胞で多く発現している
カテプシンによって切断されるため、
非がん細胞に吸収されても
薬物リリースを起こしにくい特徴を有しています。
つまり正常細胞に
影響を与えにくいリンカーと言えます。
正常細胞にも
TROP-2が発現していることを考えると
安全面で期待が持てます。
さらに搭載される抗腫瘍薬DXdは
sacituzumab govitecanに搭載されている
SN-38の1/10の濃度で
トポイソメラーゼⅠを50%阻害
することがわかっています。
つまり薬物活性が10倍強い抗腫瘍薬です。
さらにリンカーが破損し
万が一血中に解き放たれた場合、
血中半減期が短く設計されているため
早急に血中から消失します。



sacituzumab govitecanには
DARで負けているので、
DXdの強さとリンカーの安定性が
差別化ポイントになりそうですね。
その後の新データ関連
欧州臨床腫瘍学会(ESMO)で
新しいデータが発表され、
プレスリリースにて共有されています!
有効性については、Actionable 遺伝子変異のある非小細胞肺がん患者 34 名において、客観的奏効率は 35%(部分奏効12 名)で、病勢安定 は 41%(14 名)でした。また、奏効期間 中央値は9.5 ヶ月でした。
安全性については、新たな懸念は認められませんでした。主な有害事象として、吐き気と口内炎がみられました。間質性肺疾患(以下「ILD」)については、グレード 5(死亡)の 1 名が、ILD 外部判定委員会により本剤と関連のある ILD と判定されました。
引用:欧州臨床腫瘍学会(ESMO)で発表した非小細胞肺がんにおけるDS-1062/Dato-DXd の第 1 相臨床試験の最新データについて
最後に


TROP-2いかがだったでしょうか。
皆様の理解の助けになれましたら至極幸いです。
この他にも第一三共は
- 抗HER3-ADCのU3-1402
- 抗B7-H3-ADCのDS-7300
- 抗GPR20抗体のDS-6157
- 標的非開示のDS-6000
- 前述のエンハーツ
上記品目にて同様のリンカーと
DXdの組み合わせでADCを開発、発売しています。



ひとつのリンカーテクノロジーで
こんなに薬作れるなんて
すごい羨ましいですね。