今回のテーマは核酸系モダリティの最古の薬
アンチセンス核酸医薬です!
アンチセンス核酸医薬…
聞いたことはある…
という人がほとんどではないでしょうか?
でも詳しい内容や作用機序…となると
『う…』ってなるヒトいますよね?
これってある意味当然でして、
日本では2021年末までに
2種類しか承認されていないので
扱ったことがある人が少ない薬剤ではあります。
でもこれから主流となるモダリティです…
そこで今回は核酸医薬の中で最も長い歴史を持つ
アンチセンス核酸医薬の概要を
勉強しまとめてきました!
【本記事の効能効果】
・アンチセンス核酸医薬の
概要がわかります
・アンチセンス核酸医薬の
作用機序がわかります
・世界で現在発売している
アンチセンス核酸医薬がわかります
アンチセンスってそもそも何?

まずは言葉の定義から参りましょう!
というよりこの意味がわかると
察しの良い方だと
作用機序までわかってしまいます。
先に答えを言ってしまうと
センスはタンパク質情報を記録した
RNA、またはDNAのことを示しています。
 チクチク
チクチクは?って思いますよね?
もうちょっと詳しく説明します。
センス(sense)を辞書で弾くと
感覚、知覚とかある分野でのセンスといった
内容が出てきますが、
名詞の後ろの方に
『意義』とか『意義』という内容が出てきます。
これが今回のキモです。
DNAやRNAはタンパク質の
情報をコードした物質です。
DNA &RNAの構造はそのまんま
アミノ酸の並びとタンパク質の構造を意味します!
なので情報をコードしたDNA &RNAの一本鎖を
意味を持った鎖という意味を込めて
センス鎖(タンパク質情報を持った鎖)
と呼びます。
そしてセンス鎖と
鍵と鍵穴の関係になったDNAまたはRNA鎖が
今回の主役アンチセンス鎖です。
アンチセンス鎖は
タンパク質情報を記録していません。
ただ、センス鎖と鍵と鍵穴の関係になっているため
センス鎖としっかりと結合することが可能です!
タンパク質情報をコードした
センス鎖に結合することで
目的とするタンパク質を
増やしたり減らしたりして
薬効を示すのがアンチセンス核酸医薬です。
ちなみにアンチセンス核酸医薬においてセンス鎖は
mRNA(メッセンジャーRNA)または
miRNA(マイクロRNA)が基本です。
なので厳密には違いますがアンチセンス核酸医薬は
アンチmRNA核酸、またはアンチmiRNA核酸医薬
と考えると思考の整理がしやすいかと思います。



mRNAやmiRNAに結合して
薬効を示す核酸が
アンチセンス核酸医薬です
作用機序

作用機序ですが、簡単にいうと
基本的にはセンス鎖に
対応するアンチセンス鎖をあてがうことで
センス鎖に影響を与え、
タンパク質合成を調整します。
しかしながらこのシステム
大きく分けると3つに分かれます!
- RNA分解型
- スプライシング制御型
- miRNA阻害型
この3種類です!
アンチセンスを使うこと自体は同じですが
メカニズムとしては全く違いますので面白いです!



順番に解説します!
RNA分解型
まずは最古のアンチセンス医薬品
Vitraveneが使ったシステム
RNA分解型のアンチセンス核酸医薬を紹介します。
RNA分解型のアンチセンス核酸医薬の
登場人物は3種類です!
- mRNA
- アンチセンスDNA
- RNaseH
RNaseH
いきなり出てきましたね…
まずはコレをを先に解説します。



これが分かれば作用機序も
わかります。
RNaseH
読み方はRNアーゼH
RNアーぜはリボヌクレアーゼのことで
そのファミリーの中のHの名前を冠しています。



はいよくわかりませんね!
かみ砕いていきます!
リボヌクレアーゼはリボ核酸を分解する酵素です。
リボ核酸はRNAのことです。
Ribonucleic AcidでRNAです!
つまりRNA分解酵素ってことです。
その中でもRNaseHは
RNAとDNAがくっついた場合に発動する酵素です。
具体的な仕事としては
- RNAで出来た部品の合成&破壊
(RNAプライマー) - DNAに間違ってとりこまれたRNAを破壊
こんな仕事を受け持っています。
合成と破壊というと
反対の仕事をしている様に見えますが
長いRNAを破壊して
短いRNAプライマーを合成しています。
基本的には破壊する酵素です。
平たくいうと
DNAとくっ付いたRNAを
破壊し取り除くシステムが
RNaseHです。
引用元にあるように多くの生物が有している酵素で
当然ヒトも持ち合わせています。
RNaseHはRNAプライマーを作成しますが、
後述するmiRNA(micro-RNA)はRNase III Drosha
という酵素で作成されます。
この様にRNaseは短いRNAで出来た
生体部品を作るためにも活躍しています。
RNA分解型作用機序
このRNaseHを利用して
目的のRNAを破壊してやろう!というのが
RNA分解型アンチセンス核酸医薬のコンセプトです。
破壊したいmRNAと
くっつくことができる(相補的)な
1本鎖アンチセンスDNAを核内に導入し、
アンチセンスDNAと結合したmRNAが
RNaseHにより切断、破壊されることで
mRNAの働きを押さえることが出来ます。
mRNAを破壊しますので、
余計なたんぱく質を減らすために
使われる方法です。



ちょっとわかりにくいので
イメージ図で見てみます!
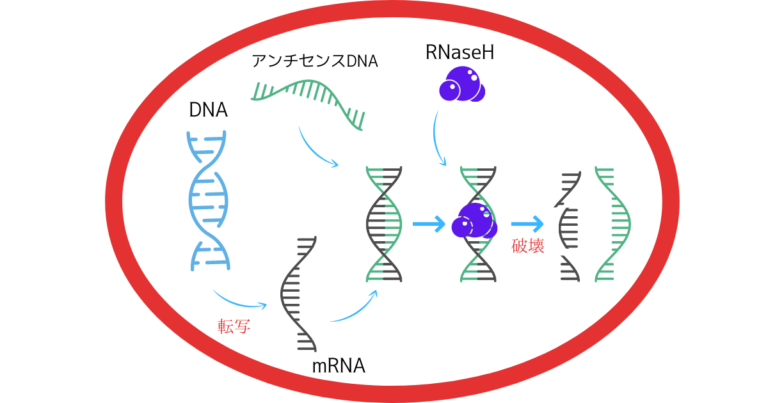

なおアンチセンスDNAには
保存キャップとして人工RNAが
最初はくっ付いています。
DNAとRNAがくっついた状態で使われますが
投与され核内に移行すると
核内に存在するRNaseHにより人工RNAも分解され
裸になったアンチセンスDNAが
ターゲットとなるm RNAを捉え
RNaseHを誘導します。



なので一本鎖DNA/RNA
という表記が薬にはなされます。
スプライシング制御型
続いて
スプライシング制御型アンチセンス核酸医薬です。
日本で2021年までに承認されている
アンチセンス核酸医薬は2種類ありますが
両方このタイプです!
一言で作用機序を書くと
RNA前駆体とスプライシング因子の結合阻害
です!!!



解説班!仕事よ!
RNA前駆体とスプライシングって?
スプライシング(splicing)日本語薬すると
『継ぎ合わせる』という意味です。
DNAから写し取られた
直後のRNA(RNA前駆体)には
タンパク質情報をもつ部分と、
実は情報を持たない部分が含まれています。
ちなみに
- 情報がある部分:エクソン
- 情報がない部分:イントロン
と呼びます!



歌のイントロには歌詞(意味、エクソン)
が入っていない!
とかこじつけて覚えちゃってください!
ここから少しの間使います。
イントロンは情報を持っておらず
タンパク質合成には不要なので、
これを切り取る作業が発生します。
切り取ってエクソンだけを『継ぎ合わせる』ことで
機能するmRNAをRNA前駆体から作成します。
この『切り取り継ぎ合わせる』作業を
スプライシングと呼びます。



この制御に介入することで
目的とするタンパク質を増やすのが
スプライシング制御型の機能です‼
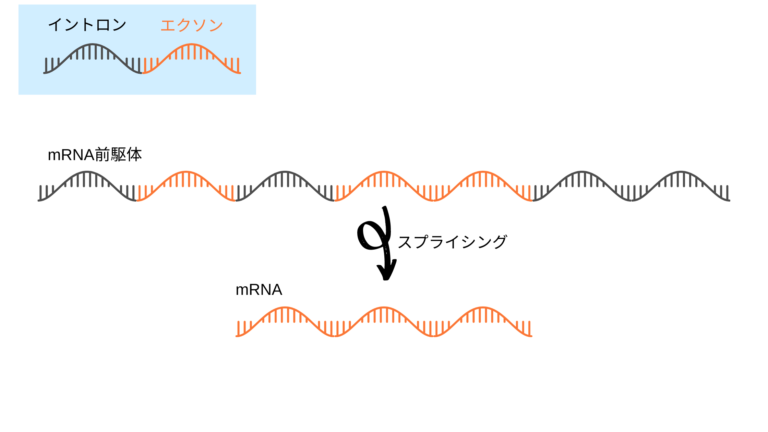

そしてスプライシング制御型の
アンチセンス核酸医薬も大きく2つに分かれます。
- エクソンスキップ型
- エクソンインクルージョン型



つづいてこの二つの
違いを見ていきます
エクソンスキップ
アンチセンスを使って
mRNAからさらにエクソンを排除することで
正常なタンパク質の機能を取り戻す方法です。
RNA前駆体に結合し
スプライシングを阻害することで
イントロンとして処理、mRNAから削除します。
もう少し詳しくいうと
ターゲットとなるエクソン部位を
アンチセンスで覆うことで
エクソンとして認識させず
イントロンと誤認させます。
イントロンと認識された
ターゲットとなるエクソンは
スプライシングによりmRNAから排除されます。
使われ方としては遺伝子が破損し、エクソン内に
タンパク質合成をやめる命令ができてしまい、
RNAが機能しない疾患の治療に使われます。
具体的には
遺伝子変異によって、エクソンに欠損が起きたときに
読み込みの順番が狂うことがあります。
順番が狂った結果、終止コドンと呼ばれる
遺伝子の途中に蛋白質を作るのを
止めてしまいなさいという配列が現れ
それ以降、正常にmRNAが
働かなくなる疾患があります。
こんなケース、そして作成するタンパク質が
少々短くなっても構わない場合では
エクソンスキップを
アンチセンスを使って行うことで
終止コドンを含むエクソンを
丸々mRNAから排除します。



文章だけだとわかりにくいと思います。
ビルテプソの作用機序動画が
非常にわかりやすいので
一度ご参照ください!
エクソンインクルージョン
エクソンスキップは
エクソンをイントロンと誤認させる方法でしたが
エクソンインクルージョンは
イントロンをエクソン、
または読み込まれないエクソンを
読み込まれるエクソンとして組み込む方法です。
誤って必要なエクソンがイントロンと誤認されて
mRNAで欠損している疾患や選択的スプライシングで読まれないエクソンが発生し機能不全のタンパク質が作られる時に使われます。
ここ!捨てますよーという命令を出す
スプライシング因子とmRNA前駆体の間に
アンチセンスが割り込み
強制的にエクソンとして認識させ
RNAに組み込みます。
こうすることで
機能するタンパク質が作れます。



コチラも同様に
動画をご参照下さい!



スプライシング制御型は
RNA分解型とは異なり
機能するタンパク質を増やす
アンチセンス核酸医薬である点もポイントです。
miRNA阻害型
つぎはmiRNA阻害型です。
作用機序を一言で表すと
miRNAとmRNAの結合阻害です。



miRNAから見ていきます!
miRNA(micro-RNA)と作用機序
miRNAって
これ自体はタンパク質に翻訳されません。
つまり、これ自体は
タンパク質情報を持っていません。
しかし重要な働きがあります。
それがmRNAの調整作用です。
過剰に発現したmRNAに結合し、
その働きを阻害することで
タンパク質生成を抑える働きがあります。
つまりはmRNAのブレーキ役です!
そこで、このブレーキ役miRNAを
アンチセンス核酸で抑えればブレーキがなくなり
mRNAがより働き
目的とするタンパク質を増やせるよね?
というシステムがmRNA阻害型です。
ちなみに
RNA分解型やスプライシング制御型は
核内で働きますが
miRNA阻害型は
細胞質で働くという違いもあります。



アンチセンスではありませんが
疾患が原因で低下し た miRNAを
化学合成したmiRNAで補うという
miRNA医薬も研究されています。


どんな薬があるの?
アンチセンス核酸医薬一覧


最後に2021年末まで発売されている
アンチセンス核酸医薬を
一覧で見ていきたいと思います。
(スマホだと表を左右にスクロールできます)
| 製品名 | 一般名 | 承認国/年 | 適応 |
|---|---|---|---|
| Vitravene | fomivirsen | 米国 1998 欧州 1999 | CMV性網膜炎 (AIDS患者) |
| Kynamro | mipomersen | 米国 2013 | ホモ接合型家族性 高コレステロール血症 |
| Exondys 51 | eteplirsen | 米国 2016 | デュシェンヌ型 筋ジストロフィー |
| Spinraza (スピンラザ) | nusinersen | 米国 2016 欧州 2017 日本 2017 | 脊髄性筋萎縮症 |
| Tegsedi | inotersen | 米国 2018 欧州 2018 | 遺伝性ATTR アミロイドーシス |
| Waylivra | volanesorsen | 欧州 2019 | 家族性 高カイロミクロン血症 |
| Vyondys 53 | golodirsen | 米国 2019 | デュシェンヌ型 筋ジストロフィー |
| Viltepso (ビルテプソ) | viltolarsen | 日本 2020 米国 2020 | デュシェンヌ型 筋ジストロフィー |
| Amondys 45 | casimersen | 米国 2021 | デュシェンヌ型 筋ジストロフィー |
日本承認は2/9製品
ちょっと少なく感じますね!
最古は1998年ですが
2016年から盛り上がっており
7製品が発売されています。(2021年まで)
そこから数えても2/7…
導入されているのが28.5%ってのは
ちょっと少なくてショックですね…
ただ、これからどんどん増えてくるのは
間違いありません。



あと製品名に数字が入るのも
面白いですね!!!
まとめ


・アンチセンス核酸医薬の概要
・アンチセンス核酸医薬の作用機序
・世界で現在発売しているアンチセンス核酸医薬
上記3点を紹介いたしました。
現在、いくつかのアンチセンス核酸医薬が
世界中で使われています。
特に、2016年から新しい薬が続々と登場していて、
これからも増えていくこと間違いなしです。
アンチセンス核酸医薬は、
病気の原因そのものにアプローチできる可能性を秘めた、
まさに次世代の治療法です。
これからの医療にどんな風に役立っていくのか、
楽しみですね!



他のモダリティ関連記事は
こちらでご覧ください!


