bnt162とは

先日、ファイザーとBioNTech、1億2000万回のbnt162 mRNAワクチン候補を日本に提供というニュースが日本中に届けられました。
さすが世界のファイザーと驚いた次第ですが、bnt162ってどんなワクチンなんだ?と気になった方も多いですよね?私もそんな人間の一人でして、今回bnt162に関して勉強してまいりました。
過去記事
そもそもmRNAワクチンって何
そもそもmRNAワクチンってなんなんだ?って話なのですが、
mRNAワクチンは抗原とするタンパク質(今回のケースでは新型コロナウイルスの一部)を製造する情報を記憶したmRNAを人体に投与することで、人体内で抗原を製造し免疫システムを刺激し抗体を産生させ、免疫を得るという物です。
メリット
- 大量製造に向いている。
- ターゲットのDNA配列がわかれば作成が可能→迅速性に優れる。
- 核内に移行せず細胞質に入るだけで効果を発揮する。
- 宿主の遺伝子情報を変更しない。そのため宿主の遺伝情報を変更せず、がん化しにくいと考えられいる。
- mRNAは非常に不安定であり、長期的には体内から消失すると考えられる。
デメリット
- 量が少ない場合タンパク質発現効率に乏しい。
- 消失し複製されないため持続性に乏しい。
- 抗体依存性感染増強の懸念がある。(2016年デング熱ワクチン死亡事件の原因とも言われている)
- そもそもテクノロジーとしては新しく多人数に使った際の安全性情報は乏しい。
Light speedプログラムでは3系統4種類のmRNAワクチンを開発中

今回、BioN Techとファイザーの開発者候補には3系統4つの候補mRNAが上がっています。
これらを統括するプログラムはLight speedという名前になっており早期開発への意気込みを感じます。
共通部分と用語解説
それぞれ紹介する前に4つに共通している部分と用語解説を簡単にさせてください。
ワクチンのターゲットはスパイクタンパク
ワクチンで生成する抗体のターゲットを最初に紹介します。
新型コロナウイルスはACE2受容体という細胞表面タンパクにスパイク部分をつかって接合し侵入します。
そのため現在作られているワクチンの多くはスパイクをターゲットに創薬されています。
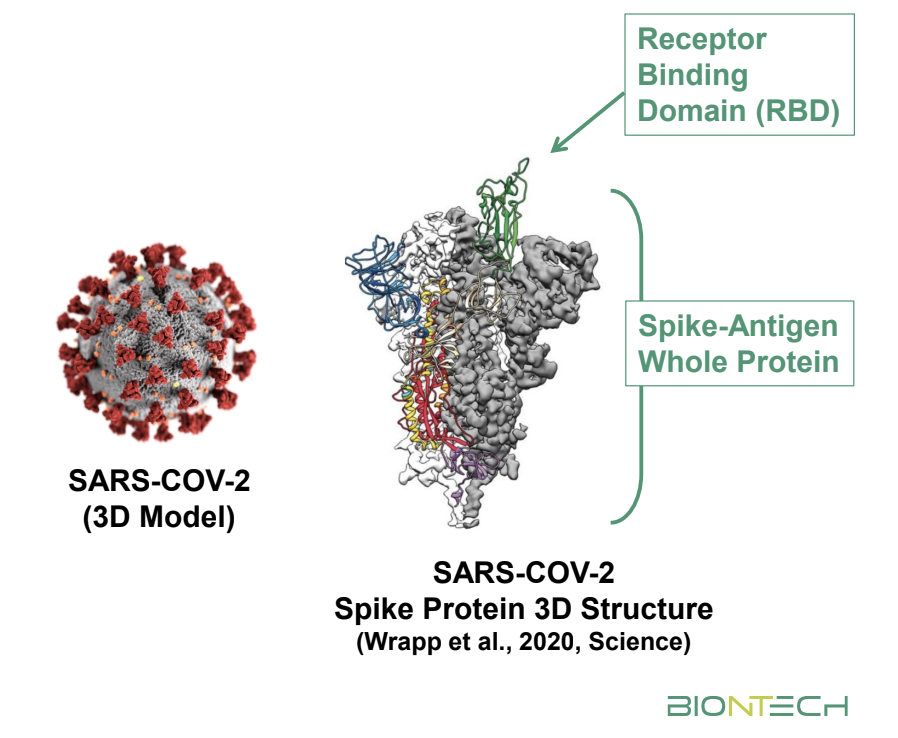
下記図の左側は新型コロナウイルス、右側はスパイクタンパク(ウイルスの赤い部分)を示しています。bnt162のターゲットはこのスパイク全体とRBD(スパイクの緑の部分)のどちらかを作るmRNAが使われています。
後述するbnt162b1はRBDを作るm RNAをベースに創薬され、bnt162b2はRBDを含むスパイクタンパク質全体を作るmRNAを使用しています。
画像引用:BioNTech bnt162 COVID-19 Vaccine
DDSは共通の脂質ナノ粒子
ドラックデリバリーシステムは全て共通の脂質ナノ粒子(Lipid nanoparticles, 以下 LNP)が使われています。
トリグリセリドや脂肪酸、ステロイドなどの生体適合性がある脂質と界面活性剤から構成されています。
生態の細胞膜はリン脂質二重膜で構成されています。細胞膜と近い物質で構成することで細胞膜と親和し細胞膜を通過してmRNAを細胞内に投入することができます。
画像引用:BioNTech bnt162 COVID-19 Vaccine
RNAの構造
次項で登場しますがRNAは基本的に以下構造をとります。
- Cap-UTR-OFR−UTR−Poly(A)
非常に端折って紹介するとCapとPoly(A)はRNAの安定性に寄与しUTRは転写に関わる分子の接合性などに関与しているとされています。そのほか色々な機能があります。
OFRはタンパク質情報が詰まっている領域です。ここが主に翻訳されます。bnt162ではスパイクタンパク情報またはRBD情報が入っています。
3系統4種類のm RNAワクチン
3系統はヌクレオチド修飾mRNAワクチン(bnt162b1,bnt162b2)、ウリジンmRNAワクチン(bnt162a1)、自己増幅mRNAワクチン(bnt162c2)があります。そのうちヌクレオチド修飾mRNAワクチンは2種類が開発されています。それぞれ紹介します。
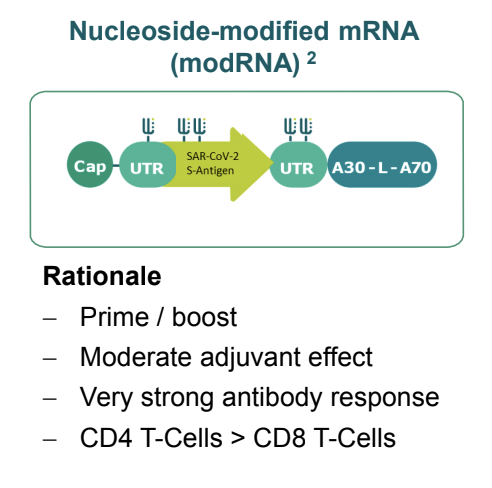
ヌクレオチド修飾mRNAワクチン(修飾ウリジンmRNAワクチン)
画像引用:BioNTech bnt162 COVID-19 Vaccine
ヌクレオチド修飾mRNAワクチンは2製品開発が進められました。それが前述のbnt162b1とbnt162b2です。
その差は前述のとおり生成するタンパク質が異なります。
- bnt162b1はスパイクタンパクの一部のRBDを作るm RNA
- bnt162b2は全スパイクタンパクを作るmRNA
なお英語で書かれている特徴を訳すと
- 複数回投与
- 中等度のアジュバント効果
- 非常に強い抗体反応
- CD4>CD8の反応
このRNAは名前の通り化学的に修飾されています。
RNAやDNAは生体内でもさまざまな修飾を受けることで遺伝情報を変化させることなく、その性質を変化させることがわかっています。ちなみにエピジェネティクスと言います。主要な変化としてはメチル化やヒストン修飾があります。
具体例としては魚類や爬虫類の雌雄決定があげられます。魚類や爬虫類では卵の時に受けた温度で雌雄が決まる種類がいます。彼らは温度によってDNA情報を変化させるわけではなくエピジェネティクスな変化で性別を変化させます。
bnt162b1並びにbnt162b2に施された修飾の目的は記載がありませんでしたが、前述のデメリットである安定性とタンパク発現率に関する物であろうことは予想できそうです。
追記:シュードウリジン化について
審査結果報告書によるとウリジン残基が N1 -メチルシュードウリジン残基に置換されているそうです。
後述しますがRNAのウラシルをウリジンに変更することで安定性を高めています。そしてさらに修飾することエピジェネティクスな変化を与えています。
シュードウリジン化は構造自体の安定化だけでなく、mRNAの解読、リボソーム機能の補助により翻訳を助けたりすることがわかっています。
安定性とタンパク発現率にかかわるもので予想通りでしたね。
開発状況
つづいてbnt162b1並びにbnt162b2の開発状況です。
ファイザー社は『ファイザーとBioNTech、COVID-19に対するmRNAワクチン候補を決定し、国際共同第2/3相試験を開始』というプレスリリースを出しています。
プレスリリースを引用します。
・両社は最適化されたSARS-CoV-2のスパイク糖タンパク全長をエンコードする修飾ヌクレオシドmRNA(modRNA)ワクチン候補であるbnt162b2を選択し、30 µgを2回接種する用法用量で第2/3相試験を実施する
・ワクチン候補と用法用量は、非臨床試験データおよび米国(C4591001)とドイツ(bnt162-01)でそれぞれ実施中の第1/2相試験データに基づき選択
・第2/3相試験の治験実施計画書は、米国食品医薬品局(FDA)のCOVID-19に対するワクチンの臨床試験デザインに関するガイダンスに完全に則っている
・最大30,000名の18~85歳の参加者を対象とする第2/3相試験を米国で開始し、世界約120施設で実施予定
・ワクチン候補bnt162b2のCOVID-19の予防効果を評価するため、SARS-CoV-2の感染率が有意に高いと予想される場所を含む地域で治験を実施
・治験が成功した場合、両社は早ければ2020年10月に規制当局に承認申請し、許可または承認が得られた場合には、2020年末までに最大1億回分、2021年末までに約13億回分を供給する計画
引用:ファイザー社プレスリリース
bnt162b2が選択され30 µgを2回接種する用法用量で第2/3相試験を実施するようです。
bnt162b1ではなくスパイクタンパク全体をを生成するbnt162b2が選ばれました。
これはb2の方が純度が高く、副反応の発生率が低かったためだそうです。
これは個人予想ですが、恐らくスパイクタンパクの一部をコードしたRNAであるb1よりも全体をコードしたb2の方が質量が重く、遠心分離を始めとした純度処理がより上手く進んだのでしょう。
ちなみにC4591001を確認するかぎり投与方法は筋肉注射となってます。海外のワクチンの多くは筋肉注射です。
一般的に筋肉注射の方が安全性、有効性ともに高いとされています。
13億回分を2021年末までに供給できる点はmRNAワクチンが大量製造に向いている事とファイザーの企業体力のすさまじさを感じさせます。
追記:第3相試験の結果発表
結果が発表され全世界で承認、使用が開始されました。日本でも2021年2月より接種がスタートしています。
簡単にP3の結果を紹介します。
米国 ニューヨーク、ドイツ マインツ、2020年12月10日 – ファイザー社(NYSE:PFE、以下「ファイザー」)およびBioNTech SE(Nasdaq: BNTX、以下「BioNTech」)は本日、両社のCOVID-19に対するmRNAワクチン候補bnt162b2の国際共同第3相試験の安全性および有効性の最終結果がThe New England Journal of Medicineに掲載されたことを発表しました。本試験に参加した43,448人(16歳以上)のうち21,720人がbnt162b2を、21,728人がプラセボを接種されました。bnt162b2は30µgを21日間隔で2回接種され、忍容性が良好であり、COVID-19予防における有効性は95%でした。
《中略》
接種時にSARS-CoV-2感染歴のなかった参加者36,523名のうち、2回目接種7日後以降のCOVID-19発症例は170例でした。そのうち8例はワクチン群、162例はプラセボ群で発現し、ワクチンの有効率は95.0%[95%信頼区間(CI: 90.3, 97.6)]でした。SARS CoV-2感染歴の有無を問わない参加者ではワクチン群で9例、プラセボ群で169例にCOVID-19が認められ、ワクチンの有効率は94.6%(95% CI: 89.9, 97.3)でした。
《中略》
bnt162b2の主な有害事象は一過性で、軽度または中等度の注射部位疼痛、疲労、頭痛で、概ね2日以内に回復しました。これらは若年成人よりも高齢者で少なく軽度でした。1回目または2回目接種後に2%以上の頻度で発現した重度(グレード3)の副反応は、疲労(3.8%)と頭痛(2.0%)でした。発熱(≥38℃)は若年者(16%)および高齢者(11%)で同程度でした。重篤な有害事象の発現頻度はワクチン群とプラセボ群で同様でした(0.6%、0.5%)。また、COVID-19関連の死亡はありませんでした。
引用:ファイザー社プレスリリース
ワクチンの有効率は95%、主な副作用は軽度または中等度の注射部位疼痛、疲労、頭痛、重度のものは疲労(3.8%)と頭痛(2.0%)という結果でした。
これはめちゃくちゃいい数字です。というよりも出来過ぎなくらいです。
参考までにインフルエンザワクチンの有効性を紹介します。
- 発症阻止効果が約30-50%
- 死亡阻止効果が約80%
bnt162b2は発症阻止効果が95%です。
この数字から死亡阻止効果は限りなく100%に近い値になりそうなことが想定されます。
めちゃくちゃよく効くワクチンという認識で間違いありません。
そして安全性情報も数万人単位で計測し、致命的なものは見つかっていません。
致命的になる可能性のあるアナフィラキシーショックも5/100万人という極々低確率です。
%にすると0.0005%です。
米国家運輸安全委員会(NTSB)によると飛行機事故で死亡する確率が0.0009%です。
飛行機事故で死ぬ確率の約1/2です。
つまりアナフィラキシーを恐れワクチンを打たないことは、飛行機事故を怖がって飛行機に乗らないことと同義でしょう。
万が一、アナフィラキシーを発症しても医療機関に滞在していればエピネフリンや輸液をはじめとした対策でリカバリーが可能です。
ワクチンを打った後に30分医療機関に待機してくれとよく言われますよね。
これはアナフィラキシーなどの急性の副反応を起こすのに30分くらいかかるためです。
つまりちゃんと30分待機していれば、万が一発症しても迅速な処置を受けることができます。
アナフィラキシーは0.0005%と極々低確率な上に
対策も確立しているので安心していいんじゃないかな?
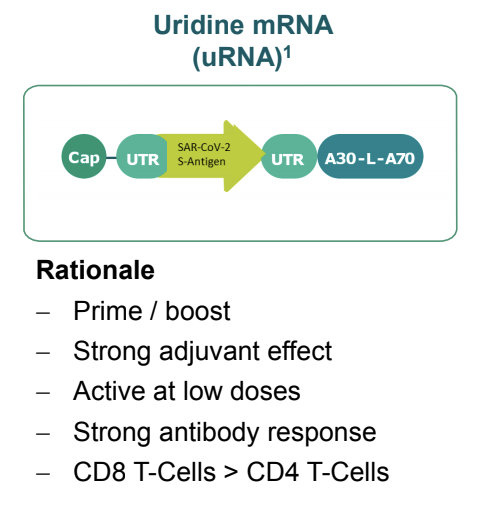
ウリジンmRNAワクチン
画像引用:BioNTech bnt162 COVID-19 Vaccine
つづいてウリジンRNAワクチンです。開発コードはbnt162a1
こちらは修飾等は受けていませんが、ウリジンを含んでいるRNAを使っています。mRNAの塩基の一つウラシルにリボースを結合させウリジンに変更することで安定性を高めています。
英語部分を翻訳すると
- 複数回投与
- 強いアジュバント効果
- 低用量で活性化
- 強い抗体反応
- CD8陽性T細胞有意の反応
CD8優位のためか、抗体反応はStrongとなっています。他の二つがVery Strongである点を考えるとこの点は劣りそうです。
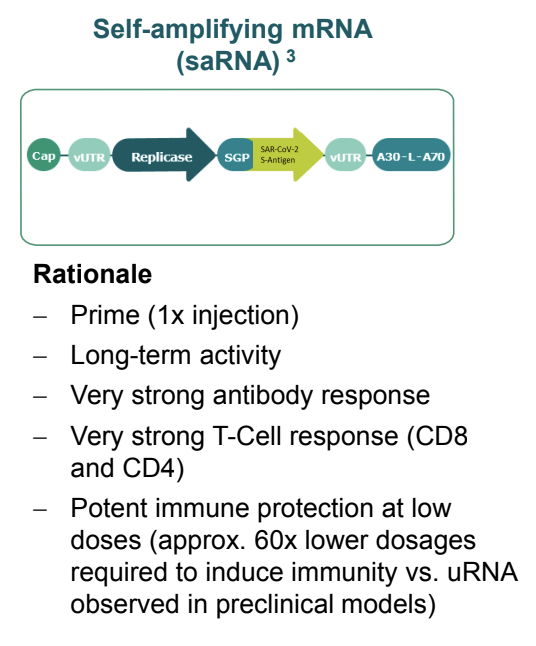
自己増幅mRNAワクチン
画像引用:BioNTech bnt162 COVID-19 Vaccine
このワクチンの最大の特徴はレプリカーゼという複製酵素を搭載している点です。レプリカーゼはもともとウイルスが自身のRNAからRNAを複製するために存在する酵素です。
これにより当RNAは自己複製能力を有すると考えられます。
mRNAワクチンのデメリットである持続性とタンパク生成能力を自己複製による量でカバーしようというアプローチです。
実際特徴を見てみても
- 1回注射
- 長時間作用型
- 非常に強い抗体反応
- CD4、CD8共に非常に強く刺激する
- 前臨床ではウリジンRNAの60分の1用量で免疫を誘発
となっており、自己複製によるメリットが感じられる内容となっています。
なお長期的にmRNAが消えないという特性です。
この特性を裏返したデメリットがどうなるのか注目していきます。
安全性という意味では懸念がありそうですね。
2/8追記:製品名決定
あとがき

ファイザー社もアストラゼネカ社もそうですが、企業体力がすごいですね。正直まだまだ臨床試験には時間がかかると思っていました。流石世界の大企業としか言いようがありません。
というか1年またずにピカイチの有効性、安全性、そして万例規模の臨床試験を終えるなんて恐怖すら覚えるスピードです。
ほんと化け物企業です。怖すぎます。ファイザーやべぇパネェです(笑)
ワープスピード計画の関連記事
- アストラゼネカ社の新型コロナウイルスワクチンAZD1222とは
- ファイザー社とBioNTechの新型コロナウイルスワクチンbnt162とは
- モデルナ社の新型コロナウイルスワクチンmRNA-1273とは【mRNAワクチンの迅速性と大量生産能力はやっぱり凄い】